Neurogénomique & Physiopathologie neuronale
Objectifs généraux

Thématiques de recherche
Déficiences intellectuelles (Dr. Laumonnier)
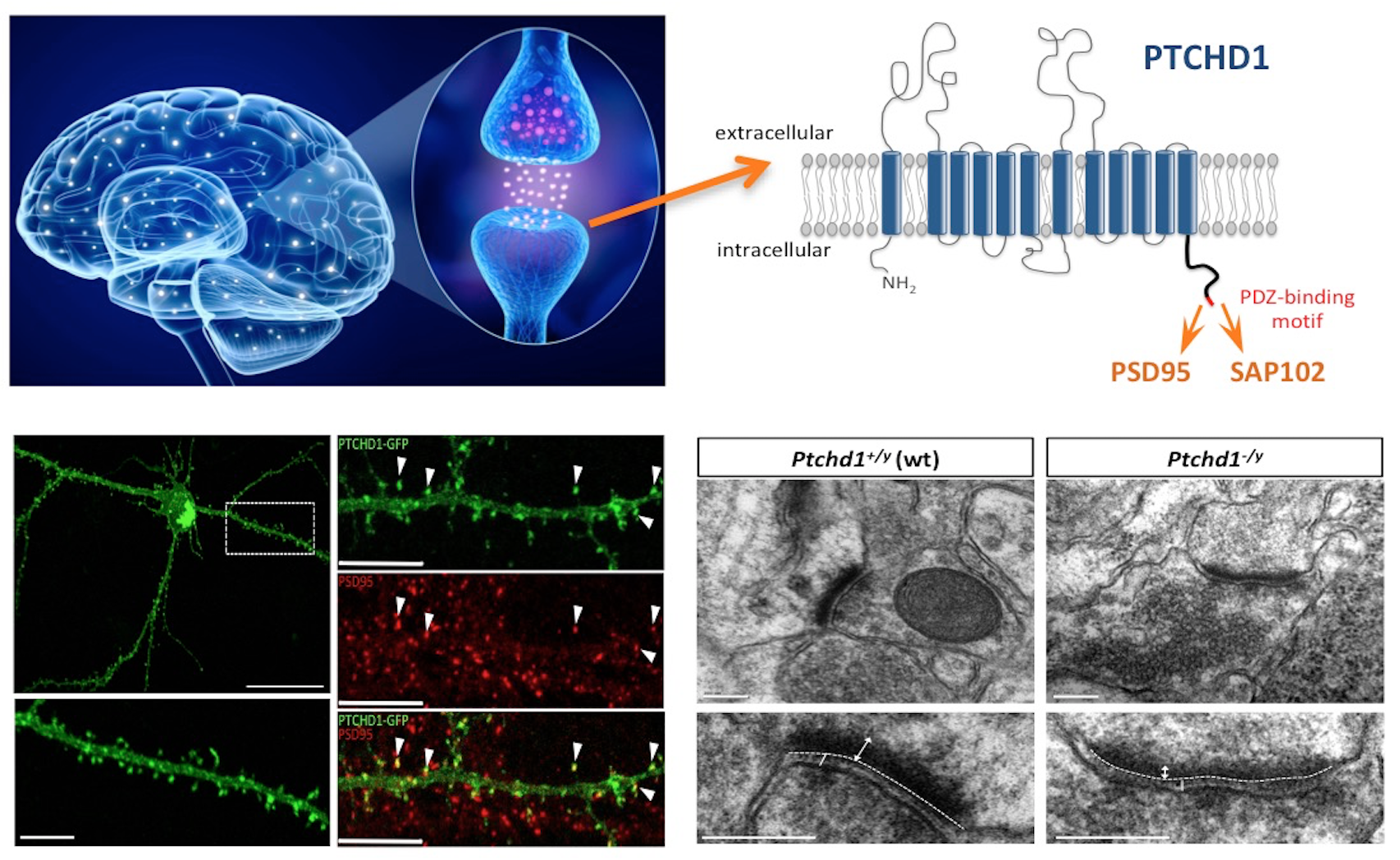
Le développement synaptique et l'activité neuronale représentent des processus fondamentaux pour l'établissement des fonctions cognitives et de communication, ainsi que pour l’apprentissage et la mémoire. L'organisation structurale et la dynamique fonctionnelle des cellules neuronales, impliquant notamment l'activité synaptique, sont particulièrement ciblées dans les troubles du développement chez l’homme tels que l’autisme et la déficience intellectuelle (DI). Le poids de l’implication de mutations génétiques y est significatif puisqu’environ 700 gènes candidats sont répertoriés à ce jour. Notre stratégie de recherche combine la génétique clinique, moléculaire et la neurogénomique fonctionnelle (modèles cellulaires neuronaux) afin de décrire les mécanismes génétiques et physiopathologiques dans ces deux pathologies présentant une comorbidité significative. Ces approches intégrées permettront de caractériser l’impact des défauts génétiques sur le neuro-développement, en particulier la formation et l’homéostasie des synapses.
Dernières publications majeures :-
Ung DC, Iacono G, Méziane H, Blanchard E, Papon MA, Selten M, van Rhijn JR, Montjean R, Rucci J, Martin S, Fleet A, Birling MC, Marouillat S, Roepman R, Selloum M, Lux A, Thépault RA, Hamel P, Mittal K, Vincent JB, Dorseuil O, Stunnenberg HG, Billuart P, Nadif Kasri N, Hérault Y, Laumonnier F. Ptchd1 deficiency induces excitatory synaptic and cognitive dysfunctions in mouse. Mol. Psychiatry. 2018 May;23(5):1356-1367.
-
Vuillaume ML, Jeanne M, Xue L, Blesson S, Denommé-Pichon AS, Alirol S, Brulard C, Colin E, Isidor B, Gilbert-Dussardier B, Odent S, Parent P, Donnart A, Redon R, Bézieau S, Rondard P, Laumonnier F, Toutain A. A novel mutation in the transmembrane 6 domain of GABBR2 leads to a Rett-like phenotype. Ann. Neurol. 2018 Feb;83(2):437-439.
Sclérose Latérale Amyotrophique (Prof. Vourc'h)
Nous abordons l’étude de la SLA par plusieurs aspects : 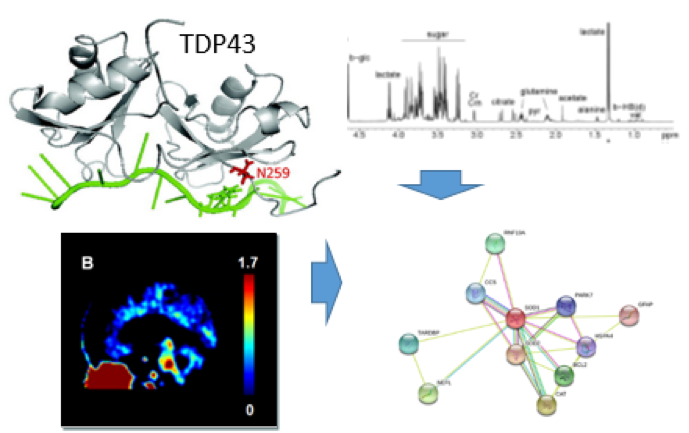
Tout d’abord nous cherchons à identifier les facteurs génétiques de la SLA par une approche multidisciplinaire en lien avec le Centre de référence sur la SLA du CHRU de Tours et la Fédération LITORALS Tours-Limoges. Nous utilisons des outils d’études pangénomiques comme la CGH array et le séquençage haut débit disponibles localement et via des consortiums nationaux (filière de soin FILSLAN) et internationaux (Programme Mine par exemple). Ensuite nous cherchons à comprendre le rôle de ces facteurs génétiques dans la physiopathologie de la SLA par des approches intégratives de génomique fonctionnelle, de métabolomique et d’imagerie cellulaire sur des cultures de motoneurones, des modèles pré-cliniques, et des fluides biologiques humains. Nous nous intéressons tout particulièrement aux rôles de ces facteurs génétiques sur l’homéostasie protéique (agrégation) et le fonctionnement de la synapse. L’ensemble de nos travaux a pour objectif de pouvoir transférer rapidement en pré-clinique et en clinique de nouveaux biomarqueurs génétiques, métaboliques, cliniques et d’imagerie en lien avec l’équipe 3, mais aussi de tester de nouvelles thérapeutiques à base d’anticorps (Labex MabImprove) ou de petites molécules chimiques.
Dernières publications majeures :
-
Madji Hounoum B, Blasco H, Coque E, Vourc'h P, Emond P, Corcia P, Andres CR. Raoul C, Mavel S. The Metabolic Disturbances of Motoneurons Exposed to Glutamate. Mol. Neurobiol. 2018 Feb 12.
-
Maurel C, Dangoumau A, Marouillat S, Brulard C, Chami A, Hergesheimer R, Corcia P, Blasco H, Andres CR, Vourc'h P. Causative Genes in Amyotrophic Lateral Sclerosis and Protein Degradation Pathways: a Link to Neurodegeneration. Mol. Neurobiol. 2018 Jan 10.
SETMAR & Glioblastome (Prof. Augé-Gouillou)
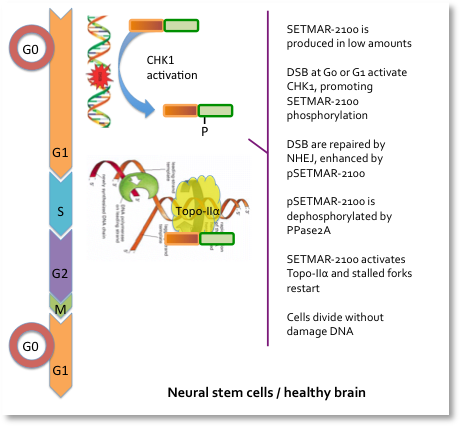
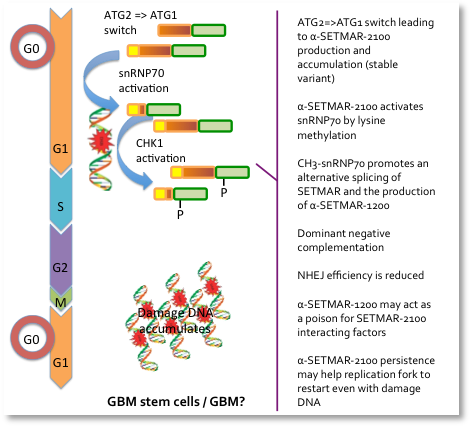
Membres de l'équipe
Directeur de l'équipe
Laumonnier F
Chercheurs
PU, MCU-PH
Andres C
Blasco H
Corcia P
De Toffol B
Toutain A
Vourc'h P
Vuillaume ML
PU, MCU
Augé-Gouillou C
Minier F
Renault S
PH
Arpin SBenz de Bretagne I
Jeanne M
Limousin N
ATER
ITA
Cherpi-Antar CGenty M
Jaillet J
Lever D
Marouillat S
Moizard MP
Ronce N
Vonwill S
Post-doctorants
Lanznaster D
Lie O
Doctorants
Clément BHalewa J
Hergesheimer R
